కాపర్(II) హైడ్రాక్సైడ్

| |
| |
| పేర్లు | |
|---|---|
| IUPAC నామము
Copper(II) hydroxide
| |
| ఇతర పేర్లు
Cupric hydroxide
| |
| గుర్తింపు విషయాలు | |
| సి.ఎ.ఎస్. సంఖ్య | [20427-59-2] |
| పబ్ కెమ్ | 164826 |
| కెగ్ | C18712 |
| SMILES | [Cu+2].[OH-].[OH-] |
| |
| ధర్మములు | |
| Cu(OH)2 | |
| మోలార్ ద్రవ్యరాశి | 97.561 g/mol |
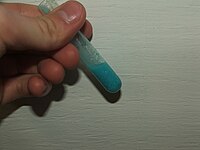
| స్వరూపం | Blue or blue-green solid |
| సాంద్రత | 3.368 g/cm3, solid |
| ద్రవీభవన స్థానం | 80 °C (176 °F; 353 K) (decomposes into CuO) |
| negligible | |
| Solubility product, Ksp | 2.20 x 10−20[1] |
| ద్రావణీయత | insoluble in ethanol; soluble in NH4OH, KCN |
| ఉష్ణగతిక రసాయన శాస్త్రము | |
| నిర్మాణము మారుటకు కావాల్సిన ప్రామాణిక ఎంథ్రఫీ ΔfH |
−450 kJ·mol−1 |
| ప్రామాణిక మోలార్ ఇంథ్రఫీ S |
108 J·mol−1·K−1 |
| ప్రమాదాలు | |
| ప్రధానమైన ప్రమాదాలు | Skin, Eye, & Respiratory Irritant |
| భద్రత సమాచార పత్రము | http://www.sciencelab.com/xMSDS-Cupric_Hydroxide-9923594 |
| జ్వలన స్థానం | {{{value}}} |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose)
|
1000 mg/kg (oral, rat) |
| సంబంధిత సమ్మేళనాలు | |
| ఇతరఅయాన్లు | {{{value}}} |
ఇతర కాటయాన్లు
|
Nickel(II) hydroxide Zinc hydroxide Iron(II) hydroxide Cobalt hydroxide |
సంబంధిత సమ్మేళనాలు
|
Copper(I) oxide Copper(I) chloride |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |
| Infobox references | |
కాపర్ (II)ఆక్సైడ్ ఒక రసాయన సమ్మేళన పదార్థం.ఇదిరాగి మూలకం యొక్క హైడ్రాక్సైడ్.ఈ సంయోగాపదార్థంలో రాగి,ఆక్సిజన్, హైడ్రోజన్ మూలకాలు ఉన్నాయి.కాపర్ (II)ఆక్సైడ్ యొక్క రసాయననిక సంకేత పదం Cu(OH)2
భౌతిక ధర్మాలు[మార్చు]
కాపర్ ఆక్సైడు లేత నీలి రంగులో,జిగటగా ఉండు రసాయన పదార్థం. స్థిరీకరించబడిన కాపర్ హైడ్రాక్సైడు అను పేరుతొ అమ్మబడునది కాపర్(II)కార్బోనేట్, కాపర్(II)కార్బొనేట్ మిశ్రమం. ఇవిసాధారణంగా కొన్నిసార్లు పచ్చరంగులో కుడా ఉండును. సజలద్రవాలలో కాపర్ (II)ఆక్సైడ్ బలహీనమైనక్షారముగా ప్రవరిస్తుంది.
చరిత్ర[మార్చు]
క్రీ,పూ.5000 నాటికే,రాగి లోహం యొక్క ధాతుశోధనం చేయ్యునప్పటికే ఈ లోహహైడ్రాక్సైడ్ పై రసవేత్తలకు అవగాహన ఉంది. ఆకాలం రసవేత్తలు మొదటిగా ఉత్పత్తి చేసిన రసాయన సమ్మేళనపదార్థం ఇదే కావొచ్చును.పూర్వకాలం నుండి బాగా తెలిసి ఉన్న పొటాషియం లేదా సోడియం ద్రావణాన్ని,, కాపర్ సల్ఫేట్ ద్రావణాలను మిశ్రమంచేసికాపర్(II) హైడ్రాక్సైడ్ తయారు చేసేవారు. 7, 18 శతాబ్దాలలో బెర్మేన్ గ్రీన్,బ్లూ వేర్డిటర్ వంటి వాటిలో రంగు దార్థంగా వ్యాపారస్థాయిలో ఉత్పత్తి చేసే వారు. ఇలా ఉత్పత్తి చేసిన రంగులను పింగాణి,, వర్ణచిత్రాల రచనలో ఉపయోగించేవారు.
స్వాభావిక లభ్యత[మార్చు]
కాపర్ (ఈ)ఆక్సైడ్ స్వాభావికంగా పలు రాగిఖనిజాలలో లభిస్తుంది.ఆజురైట్(azurite), మాలాచిట్(malachite), అంట్లేరైట్ (antlerite),, బ్రోకైన్టైట్(brochantite)వంటి రాగి ఖనిజాల్లో ఈ రసాయన సంయోగ పదార్థం లభిస్తుంది.ఈ ఖనిజాల్లో ఆజురైట్ (2CuCO3•Cu(OH)2), మాలాచిట్(CuCO3•Cu(OH)2) అనేవి రాగి లోహం యొక్క కార్బొనేటులు.అంట్లేరైట్(CuSO4•2Cu(OH)2),, బ్రోకైన్టైట్(CuSO4•3Cu(OH)2)అనేవి రాగి లోహం యొక్క సల్ఫేటులు.
కాపర్ (ఈ)ఆక్సైడ్ అతి అరుదుగా ప్రకృతిలో అమిశ్రమఖనిజంగా లభిస్తుంది.ఇది నెమ్మదిగా వాతావరణంలోని కార్బన్ డయాక్సైడ్తో చర్య చెందటం వలన మౌలిక/ప్రాథమిక కాప(II)కార్బొనేట్ గా ఏర్పడును.
సంశ్లేషణ[మార్చు]
స్వల్ప పరిమాణంలో సోడియం హైడ్రాక్సైడును క్రమంగా కాపర్(II)సల్ఫేట్(CuSO4 • 5H2O)కలపడం ద్వారా కాపర్(II)హైడ్రాక్సైడును ఉత్పత్తి చెయ్యుదురు.కొన్ని సార్లు ఈ ప్రక్రియ పద్ధతిలో అవక్షేపంగా ఏర్పడిన హైడ్రాక్సైడ్ నీటి అణువులను, సోడియం హైడ్రాక్సైడును మలినంగా కలిగి ఉండును.కాస్త శుద్ధమైన హైడ్రాక్సైడును పొందుటకై అమ్మోనియం క్లోరైడును చర్యా ద్రవాలలో కలుపుతారు. సోడియం సల్ఫెట్ లేదా మాగ్నిషియం సల్ఫేట్ కలిగిన నీటిద్రావణాన్ని విద్యుద్విశ్లేషణ చెయ్యడంవలన శుద్ధమైన కాపర్(II)హైడ్రాక్సైడును తయారు చెయ్యవచ్చును. ఈ విద్యుద్విశ్లేషణ ప్రక్రియలో రాగి కడ్డిని ఆనోడ్ గా ఉపయోగిస్తారు. తుప్పురాగి(scrape copper)నుండి ఈ ఆనోడ్ ను తయారు చెయ్యుదురు.
చెమ్మ/తేమ కలిగిన గాలితో రాగి నెమ్మదిగా చర్య వలన రాగి లోహం ఉపరితలంపైన మసగగా ఆకుపచ్చని పూతఏర్పడుతుంది. ఈ పూత/చిలుములో కాపర్ హైడ్రాక్సైడు, కాపర్ కార్బొనేట్(CuCO3) లు ఉండును.
- 2 Cu (s) + H2O (g) + CO2 (g) + O2 (g) → Cu(OH)2 (s) + CuCO3 (s)
ఈ రకపు చిలుము(patina) రాగి మిశ్రమధాతువులైన ఇత్తడి,కంచు వంటి వస్తువుల మీద కూడా ఏర్పడుతుంది.అమెరికాలో ఉదాహరణకు లిబర్టి విగ్రహం.
రసాయనచర్యలు[మార్చు]
చెమ్మ/తేమ కలిగిన కాపర్ (II)హైడ్రాక్సైడ్ పదార్థం నెమ్మదిగా రసాయన చర్యవలన,కాపర్(II)ఆక్సైడ్ ఏర్పడటం వలన నల్లగా మారును. అయితే పొడిగా(అనార్ధ్ర)ఉన్న కాపర్(II)సల్ఫైట్ సాధారణ పరిస్థితులలో వియోగం చెందదు.కాని 185°Cవరకు వేడి చేసిన విఘటన చెందును.
కాపర్(II)హైడ్రాక్సైడ్ అమ్మోనియా ద్రావణంటో రసాయన చర్య జరిపి నీలి వర్ణపు టెట్రా అమ్మైన్ కాపర్(Cu(NH3)4]2+ ) కాంప్లెక్స్ అయాను ద్రావణాన్ని ఏర్పరచును. అమ్మోనియా ద్రావనంలోని స్చెజెరుకారకం(Schweizer's reagent)అని పిలువబడు కాపర్(II)ద్రావణంలో సెల్యులోస్ కరుగుతుంది. ఈ లక్షణం కలిగి ఉన్న కారణంగా దీనిని రేయాన్,, సెల్యులోస్ ఫైబరును తయారు చెయ్యుటకు ఉపయోగిస్తున్నారు.
కాపర్ (II)హైడ్రాక్సైడ్ కొద్దిగాద్విశ్వభావయుతం(amphoteric,) కావటం వలన, క్షారములో స్వల్పంగా కరగడం వలన [Cu(OH)4]2−కేటాయాన్ ఏర్పడును
సేంద్రియ సంశ్లేషణలో కాప(II)హైడ్రాక్సైడ్ తనకంటూ ఒక ప్రత్యేక పాత్ర,ప్రాముఖ్యత కలిగిఉన్నది.కొన్ని సందర్భాలలో అరైల్ ఆమినుల(aryl amines)ను ఉత్పత్తి చెయ్యుటకైను ఉపయోగిస్తారు. 1-bromoanthraquinone లేదా-amino-4-bromoanthraquinone తోఇథైలిన్ డైఅమిన్ చర్య జరిపి, వరుస క్రమంలో1-((2-aminoethyl)amino)anthraquinone లేదా or 1-amino-4-((2-aminoethyl)amino)anthraquinone ఏర్పడుటకు ఉత్ప్రేరకంగా పనిచేయును.
కాపర్(II)హైడ్రాక్సైడ్ గదిఉష్ణోగ్రత వద్ద ఆసిడు హైడ్రాజిడేస్ను కార్బొక్సిలిక్ ఆమ్లాలుగా మార్చును.ఈ రకమైన రసాయన ప్రక్రియ ఫంక్చనల్/ క్రియాత్మక సముహాలనుండి కార్బోక్సిలిక్ ఆమ్లాలను తయారు చెయ్యుటకు చాలా అనుకూలమైనది.ఈ ప్రక్రియ బెంజోయిక్ఆమ్లం,అక్టోనిక్ ఆమ్లాలఉత్పత్తికి ప్రసస్తమైన విధానం
ఉపయోగాలు[మార్చు]
కాపర్ (II)హైడ్రాక్సైడును బెర్డెక్సుమిశ్రమానికి(Bordeaux mixture)ప్రత్నామ్యాయంగా సూక్ష్మక్రిమినాశిని( fungicide)గాను గోళక్రిమినాశిని(nematicide)గాను ఉపయోగిస్తారు.కాపర్ (II)హైడ్రాక్సైడును అప్పుడప్పుడు పింగాణి వస్తువులలలో రంగును కల్గించుటకై వాడెదరు.అలాగే కాపర్ (II)హైడ్రాక్సైడును,లాటెక్సురంగుతో కలిపి కుండిలలో పెంచు మొక్కలవేర్ల పెరుగుదలను నియంత్రించుటకు ఉపయోగిస్తారు.దీని వలన పక్కవేర్లు బాగా పెరిగి విస్తరిస్తాయి. కాపర్(II)హైడ్రాక్సైడ్ను విరివిగా ఆక్వేరియం పరిశ్రమలలో, చేపల లోని పర్నాజీవులనును, ఫ్లుక్సు,(flukes), మరైన్ ఇచ్,మెరైన్ వెల్వెట్ వంటి జీవులను చేపలు హాని జరగకుండా నాశనం చెయ్యుటకు ఉపయోగిస్తారు
ఇవికూడా చూడండి[మార్చు]
మూలాలు[మార్చు]
- ↑ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8