అణువు


అణువు అంటే తటస్థ విద్యుదావేశం కలిగి రసాయన బంధం ద్వారా కలిసి ఉండే రెండు లేదా అంతకన్నా ఎక్కువ పరమాణువుల సమూహం.[4][5][6][7][8] అయాన్ల వలె అణువులు విద్యుదావేశం కలిగి ఉండవు. తటస్థంగా ఉంటాయి.
క్వాంటం భౌతిక శాస్త్రం, సేంద్రియ రసాయన శాస్త్రం, జీవ రసాయన శాస్త్రాలలో అణువులకూ, అయాన్లకూ వ్యత్యాసం చూపరు. పాలిఅటామిక్ అయాన్లను సూచించేటప్పుడు అణువు అనే పదాన్ని వాడుతుంటారు.
వాయు గతిజ సిద్ధాంతంలో వాయు కణాలను వాటి అనుఘటకాలతో సంబంధం లేకుండా "అణువు" అనే పదాన్ని ఉపయోగిస్తారు. ఈ సందర్భంలో అణువు అనేది రెండు లేక అంతకంటే ఎక్కువ పరమాణువుల సముదాయం అనే నిర్వచనం సరికాదు ఎందుకంటే జడవాయువుల (ఉత్కృష్ట వాయువులు) అణువులు ఏక పరమాణుకాలు.
ఒక అణువు సజాతీయ పరమాణువులతో ఏర్పడవచ్చు లేదా విజాతీయ పరమాణువులతో ఏర్పడవచ్చు. ఆక్సిజన్ (O2) అణువులో రెండు ఆక్సిజన్ పరమాణువులు ఉంటాయి. అనగా ఆక్సిజన్ అణువు ద్విపరమాణుకం. రసాయన సంయోగ పదార్థమైన నీటి అణువు (H2O) రెండు హైడ్రోజన్ (ఉదజని) పరమాణువులు, ఒక ఆక్సిజన్ (ఆమ్లజని) పరమాణువుతో కలసి ఏర్పడుతుంది. అలాగే జడవాయువులు ఏక పరమాణుకాలుగా ఉంటాయి.
ఒక పదార్థం అణువుల రూపంలో ఉండటం సర్వసాధారణం. సముద్రాలు, వాతావరణం మొదలైనవి అణువుల రూపంలోనే ఉంటాయి. సేంద్రియ పదార్థాలు చాలా వరకు అణువుల రూపంలో ఉంటాయి. ప్రోటీన్లు, వాటిలో ఉండే అమైనో ఆమ్లాలు, కేంద్రకామ్లాలు, చక్కెరలు, పిండి పదార్థాలు, కొవ్వు పదార్ధాలు, విటమిన్లు మొదలైన జీవ సంబంధ పదార్థాలన్నీ అణువులతో కూడుకున్నవే. పోషక ఖనిజాలు మాత్రం సాధారణంగా అణువులు కావు.
కానీ భూమి మీద లభ్యమయ్యే ఘన పదార్థాలు మాత్రం సాధారణంగా అణువులతో ఏర్పడ్డవి కావు. నేల, ధూళి, ఇసుక, బంకమట్టి, గులకరాళ్లు, బండరాళ్లు, ద్రవరూపంలో ఉండి భూమి లోపలి భాగం, ఇంకా భూమిలో ప్రధానంగా లభించే అన్ని ఖనిజాలన్నీ ఇలాంటివే. ఇవన్నీ అనేక రసాయన బంధాలను కలిగి ఉంటాయి, కానీ గుర్తించదగిన అణువులతో తయారైనవి కావు.
లవణాలు లేదా సమయోజనీయ స్ఫటికాలు సాధారణంగా అణువులుగా ఉండవు. ఇవి తరచుగా పునరావృతమయ్యే యూనిట్ కణాలతో కూడి ఉంటాయి. ఇవి రెండు తలాలలోనూ (ద్విమితీయం) (ఉదా: గ్రాఫీన్) లేదా మూడు తలాలలోనూ (ఉదా:వజ్రం, క్వార్ట్జ్, సోడియం క్లోరైడ్) విస్తరించబడి ఉంటాయి. పునరావృతమయే యూనిట్ కణాల నిర్మాణ విధానం లోహాలకు ఉంటుంది. ఇవి లోహ బంధాలను కూడి ఉంటాయి. కనుక ఘన లోహాలు అణువులతో తయారు చేయబడవు.
పదజాలం
[మార్చు]సి. పి. బ్రౌన్ ఇంగ్లీషు - తెలుగు నిఘంటువులో Atom అనే పదానికి అణువు, రేణువు, నలుసు అనే అర్థం ఇవ్వబడింది. బూదరాజు ఆధునిక వ్యవహార కోశం, ఆంధ్రగ్రంథమాల పారిభాషిక పదకోశం, దిగవల్లి వెంకటశివరావు శాస్త్ర పరిభాష, వ్యవహార కోశము, కొండేపూడి లక్ష్మీ నారాయణ సాంకేతిక పదకోశం, ప్రెస్ అకాడమీ పత్రికా పదకోశం మొదలైనవి Atom అంటే పరమాణువు అని నిర్వచించాయి. శంకరనారాయణ నిఘంటువులో అణువు, పరమాణువు రెండూ సమానార్థకాలుగా ఇచ్చారు.[9] Molecule అనే పదానికి పైన పేర్కొన్న నిఘంటువుల్లో అణువు అనే అర్థం ఇచ్చారు.[10] తెలుగు అకాడమీ పాఠ్య పుస్తకాల్లోనూ Atom అనే పదానికి పరమాణువు అనే పదాన్ని, Molecule అనే పదానికి అణువు అనే పదాన్ని వాడారు.[11]
బంధం
[మార్చు]
అణువులు సమయోజనీయ బంధం , లేదా అయానిక బంధం ద్వారా కలిసి ఉంటాయి. ప్రకృతిలో చాలా వరకు అలోహాలు (non-metals) అణువుల రూపంలోనే ఉంటాయి. ఉదాహరణకు ఉదజని (హైడ్రోజన్) రెండు పరమాణువులు కలిగిన హైడ్రోజన్ అణువు రూపంలోనే ఉంటుంది. ఒక సమ్మేళనం రెండు లేదా అంతకన్నా ఎక్కువ మూలకాలతో ఏర్పడి ఉంటుంది.[12] ఏకపరమాణుక అణువులో ఒకే మూలకానికి చెందిన రెండు లేదా అంతకన్నా ఎక్కువ పరమాణువులు ఉంటాయి. కొంతమంది లోహ స్ఫటికాలు కూడా లోహ బంధాలచేత నిర్మితమైన పెద్ద అణువులుగా భావించవచ్చునని చెబుతారు[13] కానీ మరికొంతమంది అవి అణువుల కన్నా విభిన్నంగా ప్రవర్తిస్తాయని వాదించారు.[14]
సమయోజనీయ బంధం
[మార్చు]పరమాణువుల మధ్య ఎలక్ట్రాన్ జతలను పంచుకోవడం ద్వారా ఏర్పడిన రసాయన బంధాన్ని సమయోజనీయ బంధం అంటారు. వీటిన బంధన ఎలక్ట్రాన్ల జత (bonding pair) అని కూడా వ్యవహరిస్తారు. ఎలక్ట్రాన్లను ఈ విధంగా పంచుకోవడం ద్వారా పరమాణువుల మధ్య ఆకర్షణ వికర్షణ శక్తుల వల్ల సమతౌల్యం ఏర్పడుతుంది.[15]
అయానిక బంధం
[మార్చు]అయానిక బంధం వ్యతిరేక ఆవేశాలు కలిగిన అయాన్ల మధ్య స్థిరవిద్యుత్ ఆకర్షణ వల్ల ఏర్పడే రసాయన బంధం. ఇది అయానిక సమ్మేళనాల్లో సాధారణంగా ఏర్పడే బంధం. ఒకటి లేదా అంతకన్నా ఎక్కువ ఎలక్ట్రాన్లు కోల్పోయి ఏర్పడేవి కేటయాన్లు. ఒకటి లేదా అంతకన్నా ఎక్కువ ఎలక్ట్రాన్లను గ్రహించి ఏర్పడేవి ఆనయాన్లు.[16] సులభంగా చెప్పాలంటే కేటయాన్ లోహ పరమాణువు గానూ, ఆనయాన్ అలోహ పరమాణువుతోనూ ఏర్పడుతుంది. కానీ వీటిలో ఇంకా క్లిష్టమైన అయాన్లు కూడా ఉండవచ్చు. ఉదాహరణకు NH4+ లేదా SO42−.
సాధారణ ఉష్ణోగ్రత, పీడనాలలో ఈ బంధం వల్ల చాలా సందర్భాల్లో ఘన పదార్థాలు, కొన్ని సార్లు ద్రవ పదార్థాలు ఉత్పత్తి అవుతాయి. వీటిలో ప్రత్యేకంగా గుర్తించదగిన అణువులు ఉండవు. కానీ బాష్పీభవనం, భస్మీకరణ ప్రక్రియలో మాత్రం చిన్న అణువులు ఏర్పడవచ్చు. ఈ ప్రక్రియలో కూడా సమయోజనీయ బంధంలా కాకుండా ఎలక్ట్రాన్ బదిలీ జరుగుతుంది.
అణువు పరిమాణం
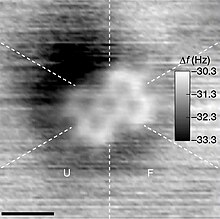
[మార్చు]చాలా వరకు అణువులు సాధారణంగా మనిషి కంటికి కనిపించవు. కానీ కొన్ని బయో పాలిమర్లలోని అణువులు మాత్రం కంటికి కనిపిస్తాయి. ఒక్క అణువును కాంతి సహాయంతో చూడటానికి వీలు పడదు. కొన్ని పరిస్థితుల్లో చిన్న అణువులు, వాటిలో ఉండే పరమాణువుల ఆకారం అటామిక్ ఫోర్స్ మైక్రోస్కోపీ ద్వారా వాటి జాడలు గుర్తించవచ్చు. అన్నింటికన్నా అతిచిన్న అణువు రెండు పరమాణువులు కలిగిన హైడ్రోజన్ అణువు. వీటి బంధం పొడవు 0.74 Å (ఆంగ్స్ట్రామ్).[17]
ఇవి కూడా చూడండి
[మార్చు]మూలాలు
[మార్చు]- ↑ Iwata, Kota; Yamazaki, Shiro; Mutombo, Pingo; Hapala, Prokop; Ondráček, Martin; Jelínek, Pavel; Sugimoto, Yoshiaki (2015). "Chemical structure imaging of a single molecule by atomic force microscopy at room temperature". Nature Communications. 6: 7766. Bibcode:2015NatCo...6.7766I. doi:10.1038/ncomms8766. PMC 4518281. PMID 26178193.
- ↑ Dinca, L.E.; De Marchi, F.; MacLeod, J.M.; Lipton-Duffin, J.; Gatti, R.; Ma, D.; Perepichka, D.F.; Rosei, F. (2015). "Pentacene on Ni(111): Room-temperature molecular packing and temperature-activated conversion to graphene". Nanoscale. 7 (7): 3263–9. Bibcode:2015Nanos...7.3263D. doi:10.1039/C4NR07057G. PMID 25619890.
- ↑ Hapala, Prokop; Švec, Martin; Stetsovych, Oleksandr; Van Der Heijden, Nadine J.; Ondráček, Martin; Van Der Lit, Joost; Mutombo, Pingo; Swart, Ingmar; Jelínek, Pavel (2016). "Mapping the electrostatic force field of single molecules from high-resolution scanning probe images". Nature Communications. 7: 11560. Bibcode:2016NatCo...711560H. doi:10.1038/ncomms11560. PMC 4894979. PMID 27230940.
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "Molecule".
- ↑ Ebbin, Darrell D. (1990). General Chemistry (3rd ed.). Boston: Houghton Mifflin Co. ISBN 978-0-395-43302-7.
- ↑ Brown, T.L.; Kenneth C. Kemp; Theodore L. Brown; Harold Eugene LeMay; Bruce Edward Bursten (2003). Chemistry – the Central Science (9th ed.). New Jersey: Prentice Hall. ISBN 978-0-13-066997-1.
- ↑ Chang, Raymond (1998). Chemistry (6th ed.). New York: McGraw Hill. ISBN 978-0-07-115221-1.
- ↑ Zumdahl, Steven S. (1997). Chemistry (4th ed.). Boston: Houghton Mifflin. ISBN 978-0-669-41794-4.
- ↑ "ఆంధ్రభారతి నిఘంటు శోధన". andhrabharati.com. Retrieved 2021-11-19.
- ↑ "ఆంధ్రభారతి నిఘంటు శోధన". andhrabharati.com. Retrieved 2021-11-19.
- ↑ అధ్యాయం - 5: పరమాణువులు, అణువులు (PDF). ప్రభుత్వ ప్రచురణ - తెలంగాణ, హైదరాబాదు. 2013. p. 70. Archived from the original (PDF) on 2021-11-19. Retrieved 2021-11-19.
- ↑ The Hutchinson unabridged encyclopedia with atlas and weather guide. Oxford, England. OCLC 696918830.
- ↑ Harry, B. Gray. Bonding in Solids (PDF). pp. 210–211.
- ↑ Finl, Academy of. "How many gold atoms make gold metal?". phys.org (in ఇంగ్లీష్). Retrieved 2021-11-22.
- ↑ Campbell, Neil A.; Brad Williamson; Robin J. Heyden (2006). Biology: Exploring Life. Boston: Pearson Prentice Hall. ISBN 978-0-13-250882-7. Retrieved 2012-02-05.
- ↑ Campbell, Flake C. (2008). Elements of Metallurgy and Engineering Alloys (in ఇంగ్లీష్). ASM International. ISBN 978-1-61503-058-3.
- ↑ Roger L. DeKock; Harry B. Gray; Harry B. Gray (1989). Chemical structure and bonding. University Science Books. p. 199. ISBN 978-0-935702-61-3.
