లిట్మస్


(అంటే ఆల్కలీన్) పరిస్థితులలో ఎరుపు లిట్మస్ కాగితం నీలంగా మారుతుంది, రంగు మార్పుతో పాటు 25°C వద్ద pH పరిధి 4.5-8.3. తటస్థ లిట్మస్ కాగితం ఊదా రంగులో ఉంటుంది.[1] Lలిట్మస్ను అదే విధంగా పనిచేసే సజలద్రవం గా కూడా తయారు చేయవచ్చు. ఆమ్ల పరిస్థితులలో ద్రావణం ఎరుపు రంగులో ఉంటుంది, క్షార పరిస్థితులలో ద్రావణం నీలం రంగులో ఉంటుంది.
లిట్మస్ మిశ్రమం CAS సంఖ్య1393-92-6ని కలిగి ఉంటుంది, 10 నుండి 15 రకాల రంగులను కలిగి ఉంటుంది. లిట్మస్లోని చాలా రసాయన భాగాలు orcein అని పిలువబడే సంబంధిత మిశ్రమంతో సమానంగా ఉంటాయి, కానీ వేర్వేరు నిష్పత్తిలో ఉంటాయి. Liṭmas’lōni cālā r orcein కి విరుద్ధంగా, లిట్మస్ యొక్క ప్రధాన భాగం సగటు పరమాణు బరువు 3300.[2] లిట్మస్పై యాసిడ్-బేస్ సూచికలు వాటి లక్షణాలకు 7-హైడ్రాక్సీఫెనాక్సాజోన్ క్రోమోఫోర్ పై ఆధారపడి ఉంటాయి.[3] లిట్మస్ యొక్క కొన్ని భిన్నాలకు, ఎరిథ్రోలిట్మిన్]] (లేదా ఎరిథ్రోలిన్), అజోలిట్మిన్, స్పానియోలిట్మిన్, ల్యూకోర్సీన్, ల్యూకాజోలిట్మిన్ వంటి నిర్దిష్ట పేర్లు ఇవ్వబడ్డాయి. అజోలిట్మిన్ ,లిట్మస్ స్ వలె దాదాపు అదే ప్రభావాన్ని చూపుతుంది.[4]
చరిత్ర
[మార్చు]లిట్మస్ను మొదటిసారిగా 1300 ADలో స్పానిష్ రసవాది అర్నాల్డస్ డి విల్లా నోవా ఉపయోగించాడు.[1] 16వ శతాబ్దం నుండి, నీలిరంగు కొన్నిపాచి(lichens)మొక్కల నుండి, ముఖ్యంగా నెదర్లాండ్స్లో సంగ్రహించబడింది.
సహజ వనరులు
[మార్చు]
లిట్మస్ వివిధ జాతుల నాచు/పాచి మొక్కలలో లో చూడవచ్చు. రంగులు రోసెల్లా టింక్టోరియా (దక్షిణ అమెరికా), రోసెల్లా ఫ్యూసిఫార్మిస్ అంగోలా, మడగాస్కర్, రోసెల్లా పిగ్మేయా' వంటి జాతుల నుండి సంగ్రహించబడతాయి. (అల్జీరియా), రోసెల్లా ఫైకోప్సిస్, లెకనోరా టార్టారియా (నార్వే, స్వీడన్), వేరియోలారియా డీల్బాటా, ఓక్రోలెచియా పరెల్లా , పర్మోట్రేమా టింక్టోరం, పర్మేలియా (పాచి )|పర్మేలియా. ప్రస్తుతం, ప్రధాన వనరులు [[రోసెల్లా మోంటాగ్నీ (మొజాంబిక్), డెండ్రోగ్రాఫా ల్యూకోఫోయా (కాలిఫోర్నియా) లు .[1]
ఉపయోగాలు
[మార్చు]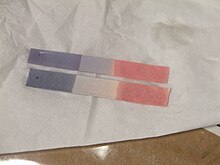
లిట్మస్ యొక్క ప్రధాన ఉపయోగం ఒక ద్రవం ఆమ్లమా లేదా ప్రాథమికమా అని పరీక్షించడం నీటిలో కరిగే వాయువులను పరీక్షించడానికి తడి లిట్మస్ పేపర్ను కూడా ఉపయోగించవచ్చు; వాయువు నీటిలో కరిగిపోతుంది, ఫలితంగా వచ్చే ద్రావణం లిట్మస్ పేపర్కు రంగులు కల్గిస్తుంది . ఉదాహరణకు, అమోనియా వాయువు, ఇది ఆల్కలీన్, ఎరుపు లిట్మస్ కాగితాన్ని నీలం రంగులో ఉంచుతుంది.
| Litmus (pH సూచిక) | ||
| pH 4.5 కంటె తక్కువ | pH 8.3 కంటె ఎక్కువ | |
| 4.5 | ↔ | 8.3 |
యాసిడ్-బేస్ రియాక్షన్ కాకుండా ఇతర రసాయన ప్రతిచర్యలు కూడా లిట్మస్ పేపర్కి రంగు-మార్పును కలిగిస్తాయి. ఉదాహరణకు, క్లోరిన్ వాయువు నీలిరంగు లిట్మస్ పేపర్ను తెల్లగా మార్చుతుంది – లిట్మస్ డై వర్ణ విహీనం అవుతుంది,[5] హైపోక్లోరైట్ అయాన్ల ఉనికి కారణంగా. ఈ ప్రతిచర్య ప్రకోపకం, అందువల్ల లిట్మస్ ఈ పరిస్థితిలో సూచికగా పనిచేయదు.లిట్మస్ పేపర్ ప్రత్యామ్నాయం గా ఒక తెల్ల కాగితం పై మందార పువ్వును రుద్ది ఆరా పెడితే లిట్మస్ పేపర్ కు ప్రత్యామ్నాయం తయారైనట్లే.
ఇవి కూడా చూడండి
[మార్చు]- Nitrazine strips - Measures pH about 4.5 to 7.5 with more precision
- pH సూచిక
- ఫినాప్తలీన్
- బ్రోమోథిమోల్ బ్లూ
- మిథైల్ ఆరెంజ్
- సార్వత్రిక సూచిక - Modern paper measures pH 1 to 14 with distinct colors for each. The color chart is usually included with the strips.
మూలాలు
[మార్చు]- ↑ 1.0 1.1 1.2 Manfred Neupert: Lackmus in Römpp Lexikon Chemie (German), January 31, 2013.
- ↑ Beecken, H.; E-M. Gottschalk; U. v Gizycki; H. Krämer; D. Maassen; H-G. Matthies; H. Musso; C. Rathjen; Ul. Zdhorszky (2003). "Orcein and Litmus". Biotechnic & Histochemistry. 78 (6): 289–302. doi:10.1080/10520290410001671362.
- ↑ H. Musso; C. Rathjen. "Orcein dyes. X. Light absorption and chromophore of litmus". Chem. Ber. 92: 751–3.
- ↑ E.T. Wolf: Vollständige Übersicht der Elementar-analytischen Untersuchungen organischer Substanzen, S.450-453, veröffentlicht 1846, Verlag E. Anton (Germany)
- ↑ UCC - Chlorine
