కాడ్మియం ఫ్లోరైడ్
| |
| పేర్లు | |
|---|---|
| IUPAC నామము
Cadmium fluoride
| |
| ఇతర పేర్లు
Cadmium(II) fluoride, Cadmium difluoride
| |
| గుర్తింపు విషయాలు | |
| సి.ఎ.ఎస్. సంఖ్య | [7790-79-6] |
| యూరోపియన్ కమిషన్ సంఖ్య | 232-222-0 |
| SMILES | F[Cd]F |
| |
| ధర్మములు | |
| CdF2 | |
| మోలార్ ద్రవ్యరాశి | 150.41 g/mol |
| స్వరూపం | grey or white-grey crystals |
| సాంద్రత | 6.33 g/cm3, solid |
| ద్రవీభవన స్థానం | 1,110 °C (2,030 °F; 1,380 K) |
| బాష్పీభవన స్థానం | 1,748 °C (3,178 °F; 2,021 K) |
| 4.35 g/100 mL | |
| ద్రావణీయత | soluble in acid insoluble in ethanol alcohol and liquid ammonia |
| నిర్మాణం | |
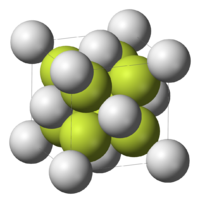
స్ఫటిక నిర్మాణం
|
Fluorite (cubic), cF12 |
| Fm3m, No. 225 | |
| ఉష్ణగతిక రసాయన శాస్త్రము | |
| నిర్మాణము మారుటకు కావాల్సిన ప్రామాణిక ఎంథ్రఫీ ΔfH |
-167.39 ± 0.23 kcal. mole-1 at 298.15 (K, C?) |
| ప్రమాదాలు | |
| ఇ.యు.వర్గీకరణ | {{{value}}} |
| R-పదబంధాలు | మూస:R45, మూస:R46, R60, R61, R25, R26, మూస:R48/23/25, R50/53 |
| S-పదబంధాలు | S53, S45, S60, S61 |
| US health exposure limits (NIOSH): | |
PEL (Permissible)
|
[1910.1027] TWA 0.005 mg/m3 (as Cd) |
REL (Recommended)
|
Ca[1] |
IDLH (Immediate danger)
|
Ca [9 mg/m3 (as Cd)] |
| సంబంధిత సమ్మేళనాలు | |
| ఇతరఅయాన్లు | {{{value}}} |
ఇతర కాటయాన్లు
|
Zinc fluoride, Mercury(II) fluoride, Copper(II) fluoride, Silver(II) fluoride, Calcium fluoride, Magnesium fluoride |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |
| Infobox references | |
కాడ్మియం ఫ్లోరైడ్ ఒక రసాయన సంయోగ పదార్థం.ఇది ఒక అకర్బన రసాయన సంయోగ పదార్థం.కాడ్మియం,, ఫ్లోరిన్ మూలకాల పరమాణువుల సంయోగం వలన కాడ్మియం ఫ్లోరైడ్ సమ్మేళనపదార్థం ఏర్పడినది.కాడ్మియం ఫ్లోరైడ్ రసాయన సంకేత పదం CdF2.నీటిలో కరుగని ఈరసాయన పదార్థాన్ని ఆక్సిజన్ సెన్సిటివ్ అప్లికేసన్లలో, అనగా లోహ మిశ్రమ ధాతుఉత్పత్తులలో ఉపయోగిస్తారు.అతితక్కువ గాఢతలో(low concentrations) (ppm ప్రమాణంలో) కాడ్మియం ఫ్లోరైడ్ ను ఇతర ఫ్లోరైడ్ సంమేలనాలను పరిమిత వైద్యచికిత్సప్రోటోకాల్లలో ఉపయోగిస్తారు. ఫ్లోరైడ్ సంయోగ పదార్థాలను సింథటిక్ ఆర్గానిక్ రసాయన కెమిస్ట్రీలో తగిన ఉపయోగాలు ఉన్నాయి. కాడ్మియం ప్రామాణిక ఎంథాల్పి -167.39 కిలో క్యాలరీలు.
భౌతిక లక్షణాలు
[మార్చు]భౌతిక స్థితి
[మార్చు]కాడ్మియం ఫ్లోరైడ్ గ్రే లేదా తెలుపు-గ్రే మిశ్రితమైన రంగును కల్గిన స్పటిక రూప ఘనపదార్థం. కాడ్మియం ఫ్లోరైడ్ అణుభారం 150.41 గ్రాములు/మోల్.[2]
సాంద్రత
[మార్చు]సాధారణ 25 °C ఉష్ణోగ్రత వద్ద కాడ్మియం ఫ్లోరైడ్ సాంద్రత 6.33 గ్రాములు/సెం.మీ3[2]
ద్రవీభవన ఉష్ణోగ్రత
[మార్చు]కాడ్మియం ఫ్లోరైడ్ రసాయన పదార్థం ద్రవీభవన స్థానం 1, 110 °C (2, 030 °F; 1, 380K) [2]
బాష్పీభవన ఉష్ణోగ్రత
[మార్చు]కాడ్మియం ఫ్లోరైడ్ సంయోగ పదార్థం యొక్క మరుగు లేదా బాష్పీభవన స్థానం 1, 748 °C(3, 178 °F;2, 021K) [2]
ద్రావణీయత
[మార్చు]కాడ్మియం ఫ్లోరైడ్ నీటిలో కరుగును.100 మి.లీ నీటిలో4.35గ్రాముల వరకు కరుగును. కాడ్మియం ఫ్లోరైడ్ ఆమ్లాలలో కరుగును.కాని ద్రవ అమ్మోనియా, ఇథనాల్/ఇథనొల్ ఆల్కహాల్ లో కరుగదు.
ఉత్పత్తి
[మార్చు]వాయుస్థితిలో నున్న ఫ్లోరిన్ లేదా హైడ్రోజన్ ఫ్లోరైడ్ లు కాడ్మియం లోహం లేదా క్లోరైడ్, ఆక్సైడ్, లేదా సల్ఫేట్ వంటి కాడ్మియం లవణాలతోచర్య ఫలితంగా కాడ్మియం ఫ్లోరైడ్ ఉత్పన్నమగును. మరొక విధానంలో కాడ్మియం కార్బోనేట్^ను 40% హైడ్రో ఫ్లోరిక్ ఆమ్లంలో కరిగించి, పిమ్మట పీడనరహిత వాతావరణంలో(వాక్యుంలో) 150 °C, దగ్గర ద్రావాన్ని వేడిచేసి బాష్పికరించడం ద్వారా కాడ్మియం ఫ్లోరైడ్ ఉత్పన్నమగును. కాడ్మియం సల్ఫైడ్ తో ఫ్లోరిన్ రసాయన చర్య ఫలితంగా కాడ్మియం ఫ్లోరైడ్ ఏర్పడును.ఈ రసాయన ప్రక్రియ చాలావేగంగా జరుగును,, చాలావరకు ఇంచుమించుశుద్ధమైన కాడ్మియం ఫ్లోరైడ్, మిగతా ఉత్పత్తి ప్రక్రియలకన్నతక్కువ ఉష్ణోగ్రత వద్ద ఉత్పాదకము ఏర్పడును.
ఉపయోగాలు
[మార్చు]ఎలక్ట్రాన్ కండక్టరులో ఉపయోగిస్తారు.నీటిలో కరుగని ఈరసాయన పదార్థాన్ని ఆక్సిజన్ సెన్సిటివ్ అప్లికేసన్లలో, అనగా లోహ మిశ్రమ ధాతుఉత్పత్తులలో ఉపయోగిస్తారు.అతితక్కువ గాఢతలో(low concentrations) (ppm ప్రమాణంలో) కాడ్మియం ఫ్లోరైడ్ను ఇతర ఫ్లోరైడ్ సంమేలనాలను పరిమిత వైద్యచికిత్సప్రోటోకాల్లలో ఉపయోగిస్తారు.[3]
ఆరోగ్యపరమైన/రక్షణ పరమైన ఇబ్బందులు
[మార్చు]తతిమ్మాఫ్లోరైడ్ రసాయన సంయోగపదార్థాలవలె కాడ్మియం ఫ్లోరైడ్ కూడా విషపూరితమైన రసాయన పదార్థం.అందువలన తగు జాగ్రత్తగా ఈ రాసాయాన్నిఉపయోగించ వలసిఉంది.ఉపయోగించు సమయంలో తగు ముందస్తు జాగ్రత్తలు తీసుకోవాలి, లేనిచో ఆరోగ్య పరమైన ఇబ్బందులున్నాయి.చర్మానికి, కళ్ళకు ఇరిటేసన్ కల్గును.కడుపులోకి వెళ్ళిన, శ్వాసించినను ప్రమాదమే. శ్వాసించిన శ్వాసకోశవ్యవస్థలో ఇరిటేసన్(ప్రకోప౦) కల్గించును.
మూలాలు/ఆధారాలు
[మార్చు]- ↑ NIOSH Pocket Guide to Chemical Hazards. "#0087". National Institute for Occupational Safety and Health (NIOSH).
- ↑ 2.0 2.1 2.2 2.3 "Cadmium Fluoride". americanelements.com. Retrieved 2016-03-28.
- ↑ "Cadmium fluoride". everything.explained.today. Retrieved 2016-03-28.
