ఆల్కేన్
ఆల్కేన్లు అనునవి కర్బన-ఉదజని సమ్మేళన పదార్థాలు. సమ్మేళనంలో కేవలం కార్బన్, హైడ్రోజన్ మూలకాలు వుండును. ఇవి సంతృప్త హైడ్రోకార్బనులు. అనగా ఆల్కేనుల కర్బన-ఉదజని గొలుసు/శృంఖలంలో ద్విబంధాలుండవు. కార్బను-కార్బను మధ్య,, కార్బనం, ఉదజని మధ్య కేవలం ఏకబంధం మాత్రమే వుండును.[1] ఆల్కేనులను గతంలో పారఫీనులని (paraffin) పిలిచేవారు. పారఫినులనగా మైనం లేదా గ్రీసు అని నిఘంటువు అర్థం.
ఉనికి
[మార్చు]వాయురూపంలో వుండు ఆల్కేనులు సహజ వాయువులో, మిగిలిన ఆల్కేనులను ముడి పెట్రోలియం (చమురు నూనె - crude oil) లో పుష్కలంగా నుండి, అంశిక లేదా అసంపూర్ణ స్వేదన క్రియ ద్వారా పొంద వచ్చును.[2]
నిర్మాణం-సాంకేతిక వివరాలు
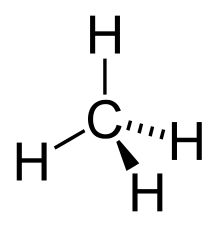
[మార్చు]ఆల్కేనులు కార్బన్-హైడ్రోజన్ రెండు మూలకాల సమ్మేళన పదార్థాలు. ఇవి వాయు, ద్రవ,, ఘనరూపంలో లభించును. ఒకే కార్బన్ పరమాణువు వుండి అది నాలుగు ఉదజని పరమాణువులతో సంయోగం చెందటం వలన మిథేన్ ఏర్పడును. ఇది వాయురూపంలో వున్న ఆల్కేను. ఆల్కేనులలో అతిచిన్న ఆల్కేను ఇది. ఆల్కేనుల సాధారణ ఫార్ములా CnH2n+2. ఆల్కేనులోని సమ్మేళనాలన్నియు సంతృప్త హైడ్రోకార్బనులు. కార్బనులమధ్య,, హైడ్రోజనులమధ్య ఏక బంధం మాత్రమే వుండును. ఆల్కేనులను మజ్జాయౌగిక (Aliphatic compounds) సమ్మేళనాలని కూడా అంటారు. పురాతన గ్రీకుభాషలో అలిఫాటిక్ ఆనగా నూనె (oil), లేపన మందు (ointment) అని భావం. మరొక అర్థంలో అరోమాటిక్ వలయాన్ని కలిగివున్న సమ్మేళనాలను మినహాయించి మిగిలిన పెట్రోలియం ఉత్పత్తులు. ఆల్కేనులు సమశ్రేణికమైన (homologous) సమ్మేళనములు. అనగా ఒక అల్కేనుకు మరో ఆల్కేనుకు తేడా ఒక ( CH2) సమూహాము . అణుభారమైనచో ఒక ఆల్కేనుకు మరో ఆల్కేనుకు అణుభారం తేడా 14.03 వుంటుంది.
ఆల్కేనులు సంతృప్త హైడ్రోకార్బను సమ్మేళనాలు అయ్యినప్పటికి రూపాలలో ఏర్పడుతాయి. కొన్ని సాధారణ సరళ శృంఖలరూపంలో ( linear) ఏర్పడివుండగా, మరికొన్ని శాఖాయుతములు (branched) . అనగా ప్రధాన ఉదజని కర్బన గొలుసుకు ప్రక్కలకు వ్యాపించి కొమ్మలవలె సంతృప్త హైడ్రోకార్బను శృంఖలాలు అనుసంధానించబడి వుండును. ఈ రెండు రూప నిర్మాణాలేకాకుండ మూడో రకం చక్రీయ రూపం (cyclic structure) . సాధారణ సరళ శృంఖల ఆల్కేనుల ఫార్ములా CnH2n+2.కొమ్మలు కలిగివున్న ఆల్కేనుల ఫార్ములా CnH2n+2, n>3,, చక్రీయ నిర్మాణమున్న ఆల్కేనుల సాంకేతిక రచన CnH2n, n>2. మూడవ రకమైన ఆల్కేనులను చక్రీయ ఆల్కేనులు (cycloalkanes) అనికూడా అంటారు. చక్రీయ ఆల్కేనులు మిగిలిన ఆల్కేనులకన్నరెండు ఉదజని కార్బనులను తక్కువగా కలిగివున్నప్పటికి, అవి ద్విబంధాలను కలిగివుండకపోవటం వలన వీటిని ఆల్కేనులుగానే భావిస్తారు.
సరళ శృంఖల ఆల్కేనులు
[మార్చు]
హెక్సేన్C6H14
ఇవి నిడుపైన, ఒకే వరుస క్రమంలో హైడ్రోకార్బను గొలుసు వున్న ఆల్కేనులు.వీటిని ఆంగ్లంలో linear Alkane లు అనిఅందురు.సరళ శృంఖల సౌష్టవం లేని సమాంగతాలున్న ఆల్కేనుల పదం ముందు n- (normal) అనే ఆక్షరాన్ని ఉంచెదరు.ఇది సరళ శృంఖల, కొమ్మలున్న ఆల్కేనుల తేడాను తెలియ పరచును.
ఈ శ్రేణికి చెందిన కొన్ని ఆల్కేనుల పేర్లు అందులోని సమ్మేళన మూలకాల సంఖ్యా వివరణ;
- మిథేన్:CH4:ఒకకార్బను, 4 హైడ్రోజన్ పరమాణులు ఉన్నాయి.
- ఇథేన్:C2H6:2 కార్బనులు, 6 ఉదజని పరమాణువులు.
- ప్రొపేన్:C3H8:3 కార్బనులు, 8 హైడ్రోజన్ పరమాణువులు.
- బ్యుటేను:C4H10:4కార్బనులు, 10 హైడ్రోజన్ పరమాణువులు.
- పెంటేన్:C5H12:5 కార్బనులు, 12 ఉదజని పరమాణువులు.
- హెక్సేను:C6H14: 6 కార్బనులు, 14 ఉదజని పరమాణువులు.
మిథేన్ నుండి బ్యుటేన్ వరకు వాటి పేర్లు మిథనాల్, ఇథనాల్, ప్రొపనాల్,, బ్యుటనాల్ లనుండి వచ్చినవి.5 కన్న కార్బనులు ఉన్న ఆల్కేను లకు ఆల్కేనులలోని కార్బనులసంఖ్య ముందుమాటగా వుంచి, చివర ఏన్ (-ane) చేర్చి పిలిచెదరు.కార్బనులసంఖ్య లపదం సాధారణంగా గ్రీకు పదం అయ్యివుండును. 9 కార్బనులను కలిగిన నోనేన్ (nonane) యొక్క ముందుమాటను లాటిన్ భాషనుండి గ్రహించారు.
సమాంగతములు/ఐసోమరులు
[మార్చు]ఒకే రకమైన ఆణుసంకేతం (molecular formula) కలిగివుండి, భిన్నమైన అణుసౌష్టవం (నిర్మాణం) చూపించు పదార్థాలను/సమ్మేళనాలను మొదటి సమ్మేళనం/పదార్థం యొక్క సమాంగతము/ఐసోమరు (Isomer) అనిఅందురు.[3] ఎటువంటి శాఖలు/కొమ్మల్ లేకుండ, సరళ శృంఖలం కలిగివున్న ఆల్కేనును n-ఐసోమరు అంటారు.n-అనగా నార్మల్ (normal, అనగా సాధారణమైన ఆల్కేను, మిగిలినవి దీనియొక్క ఐసోమరులుగా భావిస్తారు.మూడు వరకు కార్బనులను ఆల్కేనులకు ఎటువంటి ఐసోమరులు లేవు.అటుపిమ్మట వరుస క్రమంలో వున్న అన్ని ఆల్కేనులకు సమాంగతములు ఉన్నాయి. ఆల్కేనులో వున్న కార్బనుల సంఖ్య పెరిగే కొలది సదరు అల్కేను యొక్క సమాంగతములు కూడా పెరుగును[4].క్రింద కొన్ని ఆల్కేనులు వాటి సమాంగతముల వివరాలు ఇవ్వబడినవి.
ఆల్కేనులు, వాటి సమాంగతములు
- C1:ఐసోమరులు లేవు:మీథేన్
- C2:ఐసోమరులు లేవు:ఇథేన్
- C3:ఐసోమరులు లేవు:ప్రొపేన్
- C4:2 ఐసోమరులు:n-బ్యుటేన్, అసోబ్యుటేన్
- C5:3 ఐసోమరులు:పెంటేన్, ఐసోపెంటేన్, న్యూయో పెంటేన్ (neo pentane)
- C6:5 ఐసోమరులు:హెక్సేన్;2-మైథైల్ పెంటేన్;3-మిథైల్ పెంటేన్;2, 3-డైమిథైల్ బ్యుటేన్;2, 2-డైమిథైల్ బ్యుటేన్.
- C12:355 ఐసోమరులు
- C32:27, 711, 253, 769 ఐసోమరులు
- C60:22, 158, 734, 535, 770, 411, 074, 184 ఐసోమరులు.
కొమ్మలు కలిగిన ఆల్కేనుల యొక్క ఐసోమరులు దర్పణ ప్రతిబింబరూపంలో (chiral) ఏర్పడును.
ఆల్కేనుల భౌతిక గుణగణాలు
[మార్చు]- అన్ని అల్కేనులు రంగు లేనివి, వాసన లేనివి.[4] మొదటి నాలుగు ఆల్కేనులు వాయువులు.5వ కార్బను నుండి 16 కార్బనులు వరకు ఆల్కేనులు ద్రవాలు, ఆతరువాత నుండి ఆల్కేనులు ఘనరూపంలో ఉన్నాయి.
- ఆల్కేనులు నీటిలో కరుగవు.కాని హైడ్రోకార్బను ద్రావణులలో కరుగును.[5]
| ఆల్కేన్ | సంకేతం | బాష్పీభవన ఉష్ణోగ్రత [°C] | ద్రవీభవన ఉష్ణోగ్రత [°C] | సాంద్రత [g·cm−3] (20 °Cవద్ద) |
| మిథేన్ | CH4 | -162 | -182 | వాయువు |
| ఇథేన్ | C2H6 | -89 | -183 | వాయువు |
| ప్రొపేన్ | C3H8 | -42 | -188 | వాయువు |
| బ్యుటేన్ | C4H10 | 0 | -138 | వాయువు |
| పెంటేన్ | C5H12 | 36 | -130 | 0.626 (ద్రవం) |
| హెక్సేన్ | C6H14 | 69 | -95 | 0.659 (ద్రవం) |
| హెప్టేన్ | C7H16 | 98 | -91 | 0.684 (ద్రవం) |
| ఆక్టేన్ | C8H18 | 126 | -57 | 0.703 (ద్రవం) |
| నొనేన్ | C9H20 | 151 | -54 | 0.718 (ద్రవం) |
| డెకేన్ | C10H22 | 174 | -30 | 0.730 ( ద్రవం) |
| అన్డెకేన్ | C11H24 | 196 | -26 | 0.740 (ద్రవం ) |
| డొడెకేన్ | C12H26 | 21 | -10 | 0.749 (ద్రవం) |
| Hexadecane | C16H34 | 281 | 18 | 0.773 |
| Icosane | C20H42 | 343 | 37 | ఘనస్థితి |
| Triacontane | C30H62 | 450 | 66 | ఘనస్థితి |
| Tetracontane | C40H82 | 525 | 82 | ఘనస్థితి |
| Pentacontane | C50H102 | 575 | 91 | ఘనస్థితి |
| Hexacontane | C60H122 | 625 | 100 | ఘనస్థితి |
రసాయనిక చర్యలు
[మార్చు]- ఆల్కేనులను గాలితో లేదా ఆక్సిజనుతో సంపూర్ణంగా దహనంచెందించినప్పుడు/ మండించినప్పుడు బొగ్గుపులుసు వాయువు, నీరు, ఉష్ణం ఏర్పడును.[6]
ఆల్కేనులనుండి ఉత్పత్తులు
[మార్చు]పొడవైన శృంఖలం వున్న ఆల్కేనుల హైడ్రోకార్బను శృంఖలాన్ని ఛేదించడం (craking) వలన తక్కువ పొడవున్న హైడ్రోకార్బను సమ్మేళనాలను సృష్టించవచ్చును.ఈ చర్యను ఆంగ్లంలో క్రాకింగ్ అందురు.ఈ క్రాకింగ్ చర్యను ఎదైన ఒక ఉత్ప్రేరకం (catalyst) ను ఉపయోగించి లేదా అధిక ఉష్ణోగ్రత, వత్తిడి వద్ద ఉత్ప్రేరకం లేకుండ/ ఉపయోగించకుండ కూడా జరుపవచ్చును.ఈ విధంగా పొడవైన కార్బన్-ఉదజని శృంఖలం/సంకెల వున్న ఆల్కేనులకు క్రాకింగ్ (విడగొట్టి/ఛేదించి) తక్కువ పొడవున్న శృంఖలాలున్న హైడ్రోకార్బనులను సృష్టించడం జరుగుతుంది.ఈ విధంగా ఏర్పడిన హైడ్రోకార్బను సమ్మేళనాలు కొన్ని ద్విబంధం కలిగివుండును.ద్విబంధం కలిగివుండటం ఆల్కీన్ (alkene) ల స్వభావం.అల్కేనులను క్రాకింగ్ చెయ్యడం వలన అల్కేనులు, ఆల్కీన్ లు ఏర్పడును.[7] ఉత్ప్రేరకం లేకుండగా ఆల్కేనులను విడగొట్టు ప్రక్రియను ఉష్ణ/తాప విచ్చేధన (Thermal craking) అంటారు.ఉత్ప్రేరక విఛ్ఛేధన ప్రక్రియలో జియోలిట్ (zeolite) అనే ఉత్ప్రేరకాన్ని ఉపయోగిస్తారు.ఈ జియోలిట్ అనునది అల్యూమినియం, సిలికాన్,, ఆక్సిజన్ లసంయోగం వలన రూపొందుతుంది.ఇది ధనగుణాత్మకత ఆయాన్ (ion) ను కలిగివుండును.పొడవైన హైడ్రోకార్బన్ శృంఖలాన్ని ( సాధారణంగా15 లేదా అంతకు మించి కార్బనులను) కలిగిన ఆల్కేనులను 5000C వరకు వేడి చేసి, జియోలిట్ ఉత్ప్రేరకం మీదుగా ప్రసరించినప్పుడు ఆల్కేన్ శృంఖల విచ్ఛేదన జరుగును.
ఉదా:
ఉష్ణ/తాప విచ్ఛేదన ప్రక్రియలో 70కిలో/సెం, మీ2 వత్తిడి వద్ద ఆల్కేనును 450-750 °C వరకు వేడిచెయ్యడం వలన ఆల్కేను శృంఖల ఛేదన జరుగుతుంది.తాప విచ్ఛేదన ప్రక్రియలో అధిక ప్రమాణంలో ద్విబంధాలున్న ఆల్కీనులు ఏర్పడు అవకాశం మెండు.
ఉపయోగాలు
[మార్చు]- వాయురూపంలో వున్న ఆల్కేనులను ఇళ్ళలో,, వాహనాలలో ఇంధనంగా వాడెదరు.
- హేక్సేనును నూనె గింజల నుండి, నూనెపిండి (oil cake) నూనెను తీయు సాల్వెంట్ ఎక్సుట్రాక్షన్ ప్లాంట్ అను పరిశ్రమలలో ద్రావణి (solvent) గా వినియోగిస్తున్నారు.
ఇవికూడా చూడండి
[మార్చు]బయటి లింకులు
[మార్చు]- https://web.archive.org/web/20140221081142/http://hyperphysics.phy-astr.gsu.edu/hbase/organic/alkane.html
- http://chemwiki.ucdavis.edu/Organic_Chemistry/Hydrocarbons/Alkanes
మూలాలు/ఆధారాలు
[మార్చు]- ↑ "Alkanes". chemwiki.ucdavis.edu/. Retrieved 2013-11-26.
- ↑ "Fuels from crude oil". bbc.co.uk. Retrieved 2013-11-26.
- ↑ "Isomers". chemed.chem.purdue.edu/. Retrieved 2013-11-26.
- ↑ 4.0 4.1 "PHARMACEUTICAL CHEMISTRY" (PDF). nsdl.niscair.res.in/. Archived from the original (PDF) on 2013-10-29. Retrieved 2013-11-26.
- ↑ "Physical Properties of Alkanes". ucdavis. Archived from the original on 2013-12-19. Retrieved 2013-11-26.
- ↑ "Alkane Types and structures". petroleum.co.uk. Archived from the original on 2013-10-06. Retrieved 2013-11-26.
- ↑ "CRACKING ALKANES". chemguide.co.uk. Archived from the original on 2013-07-21. Retrieved 2013-11-26.