అమ్మోనియం సైనైడ్
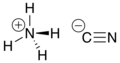
| |||
| |||
| గుర్తింపు విషయాలు | |||
|---|---|---|---|
| సి.ఎ.ఎస్. సంఖ్య | [12211-52-8] | ||
| పబ్ కెమ్ | 159440 | ||
| SMILES | [C-]#N.[NH4+] | ||
| |||
| ధర్మములు | |||
| NH4CN | |||
| మోలార్ ద్రవ్యరాశి | 44.0559 g/mol | ||
| స్వరూపం | colourless crystalline solid | ||
| సాంద్రత | 1.02 g/cm3 | ||
| బాష్పీభవన స్థానం | 36 °C (97 °F; 309 K) | ||
| very soluble | |||
| ద్రావణీయత | very soluble in alcohol | ||
| సంబంధిత సమ్మేళనాలు | |||
| ఇతరఅయాన్లు | {{{value}}} | ||
ఇతర కాటయాన్లు
|
Sodium cyanide Potassium cyanide | ||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |||
| Infobox references | |||
అమ్మోనియం సైనైడ్ ఒక రసాయనిక సంయోగ పదార్థం. ఇది అస్థిరమైన అకర్బన సమ్మేళన పదార్థం. ఈ సంయోగ పదార్థం యొక్క రసాయనిక ఫార్ములా NH4CN.
భౌతిక ధర్మాలు
[మార్చు]అమ్మోనియం సైనైడ్ ఒక రంగులేని చతుర్క్కోణ స్పటిక ఘన పదార్థం.[1] ఈ సంయోగ పదార్థం యొక్క అణుభారం 44.055 గ్రాములు/మోల్.[2] అమ్మోనియం సైనైడ్ సాంద్రత 1.02 గ్రాములు/సెం.మీ3. ఈ సంయోగ పదార్థం యొక్క భాస్పిభవన ఉష్ణోగ్రత 36 °C. అమ్మోనియం సైనైడ్నీటిలో, ఆల్కహాల్లో కరుగుతుంది.
రసాయన చర్యలు
[మార్చు]అమ్మోనియం సైనైడ్ వియోగం చెందడం వలన అమ్మోనియా, హైడ్రోజన్ సైనైడ్ ఏర్పడును. వియోగ ఫలితంగా తరచుగా నల్లని హైడ్రోజన్ సైనైడ్ పాలిమర్ ఏర్పడును.
- NH4CN → NH3 + HCN
అమ్మోనియం సైనైడ్ ద్రావణం లోహ లవణాలతో చర్య వలన ఉభయ వియోగం చెందును. గ్లైఅక్షల్ (glyoxal) తో చర్య వలన అమినోఅసిటిక్ ఆమ్లాన్ని (glycine) ఏర్పరచును.
- NH4CN + (CHO)2 → NH2CH2COOH + HCN
అలాగే కిటోన్సుతో చర్య ఫలితంగా అమినో నైట్రైల్స్ (aminonitriles) ఏర్పరచును.
- NH4CN + CH3COCH3 → NH2CH2CH2CH2CN + H2O
ఉత్పత్తి
[మార్చు]తక్కువ ఉష్ణోగ్రత వద్ద సజల అమ్మోనియాలో హైడ్రోజన్ సైనైడ్ను బబ్లింగ్ చెయ్యడం ద్వారా అమ్మోనియం సైనైడ్ను ఉత్పత్తి చెయ్యుదురు.
- HCN + NH3(aq) → NH4CN(aq)
కాల్షియం సైనైడ్ తో అమ్మోనియం కార్బోనేట్ రసాయనిక చర్య జరిపిన అమ్మోనియం సైనైడ్ఏర్పడును.
- Ca(CN)2 + (NH4)2CO3 → 2 NH4CN + CaCO3
పొడి (dry) స్థితిలో ఉన్న పొటాషియం సైనైడ్ లేదా పొటాషియం పెర్రో సైనైడ్,, అమోనియం క్లోరైడ్ మిశ్రమాన్ని వేడి చేసి, ఆవిరి రూపంలో వెలువడిన అమ్మోనియం సైనైడ్ను స్పటికాలుగా మారునట్లు చల్లార్చటం ద్వారా కూడాతయారు చెయ్య వచ్చును.
- KCN + NH4Cl → NH4CN + KCl
విష స్వభావం
[మార్చు]అమ్మోనియం సైనైడ్ ద్రవంగా లేదా ఘన పదార్థంగా అత్యంత విషకారి.జీర్ణాశయంలో చేరిన మరణం సంభవించును. ఘన రూప అమ్మోనియం సైనైడ్ ప్రభావానికి గురైన ఇది అత్యంత ప్రమాదకరమైన హైడ్రోజన్ సైనైడ్,, అమ్మోనియాగా విఘటన చెందటం వలన చాలా ప్రమాదకరం.
రసాయన విశ్లేషణ
[మార్చు]అమ్మోనియం సైనైడ్లో ఉన్న మూలకాల నిష్పతి :హైడ్రోజన్ ( H) : 9.15%, కార్బన్ (C) : 27.23%, నత్రజని (N) : 63.55%.
మూలాలు
[మార్చు]- ↑ "Ammonium Cyanide". matweb.com. Retrieved 2015-07-27.
- ↑ "Ammonium Cyanide". pubchem.ncbi.nlm.nih.gov. Retrieved 2015-07-27.

