బెరీలియం క్లోరైడ్

| |
| పేర్లు | |
|---|---|
| IUPAC నామము
Beryllium chloride
| |
| గుర్తింపు విషయాలు | |
| సి.ఎ.ఎస్. సంఖ్య | [7787-47-5] |
| పబ్ కెమ్ | 24588 |
| ఆర్.టి.ఇ.సి.యస్. సంఖ్య | DS2625000 |
| SMILES | [Be+2].[Cl-].[Cl-] |
| |
| ధర్మములు | |
| BeCl2 | |
| మోలార్ ద్రవ్యరాశి | 79.9182 g/mol[1] |
| స్వరూపం | White or yellow crystals |
| సాంద్రత | 1.899 g/cm3, solid |
| ద్రవీభవన స్థానం | 399 °C (750 °F; 672 K) |
| బాష్పీభవన స్థానం | 482 °C (900 °F; 755 K) |
| 15.1 g/100 mL (20 °C) | |
| ద్రావణీయత | soluble in alcohol, ether, benzene, and pyridine slightly soluble in chloroform and sulfur dioxide |
| నిర్మాణం | |
స్ఫటిక నిర్మాణం
|
hexagonal |
| polymer | |
| ఉష్ణగతిక రసాయన శాస్త్రము | |
| నిర్మాణము మారుటకు కావాల్సిన ప్రామాణిక ఎంథ్రఫీ ΔfH |
−6.136 kJ/g or -494 kJ/mol |
| దహనక్రియకు కావాల్సిన ప్రామాణీక ఎంథ్రఫీ ΔcH |
16 kJ/mol |
| ప్రామాణిక మోలార్ ఇంథ్రఫీ S |
63 J/mol K |
| విశిష్టోష్ణ సామర్థ్యం, C | 7.808 J/K or 71.1 J/mol K |
| ప్రమాదాలు | |
| Lethal dose or concentration (LD, LC): | |
LD50 (median dose)
|
86 mg/kg (rat, oral) |
| US health exposure limits (NIOSH): | |
PEL (Permissible)
|
TWA 0.002 mg/m3 C 0.005 mg/m3 (30 minutes), with a maximum peak of 0.025 mg/m3 (as Be) |
REL (Recommended)
|
Ca C 0.0005 mg/m3 (as Be) |
IDLH (Immediate danger)
|
Ca [4 mg/m3 (as Be)] |
| సంబంధిత సమ్మేళనాలు | |
| ఇతరఅయాన్లు | {{{value}}} |
ఇతర కాటయాన్లు
|
Magnesium chloride Calcium chloride Strontium chloride Barium chloride Radium chloride |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |
| Infobox references | |
బెరీలియం క్లోరైడ్ ఒక అకర్బన సంయోగపదార్థం. ఈ సంయోగపదార్థం రసాయనిక సంకేతపదం BeCl2.బెరీలియం, క్లోరిన్ పరమాణువు ల సంయోగం వలన బెరీలియం క్లోరైడ్ రసాయన సమ్మేళనపదార్థం ఏర్పడినది.
భౌతిక ధర్మాలు
[మార్చు]బెరీలియం క్లోరైడ్ రంగులేనటువంటి రసాయన పదార్థం.కొన్ని సార్లు తెల్లగా, లేదా పసుపురంగు స్పటికారంలో కుడా ఉండును[1]. బెరీలియం క్లోరైడ్ ఆర్ద్రతాకర్షకత కలిగిన ఘనపదార్థం.పలు దృవియ ద్రావణులలో కరుగు తుంది.బెరీలియం క్లోరైడ్ యొక్క భౌతికధర్మాలు ఎక్కువగా అల్యూమినియం క్లోరైడ్ ను పోలిఉండును. బెరీలియం క్లోరైడ్ ద్రవీభవన స్థానం405°C, బాష్పీభవన స్థానం520°C[2].సాంద్రత 1.899 గ్రాములు/సెం.మీ3[3]
నిర్మాణం-సంశ్లేషణ
[మార్చు]అత్యధిక ఉష్ణోగ్రత వద్ద బెరీలియం లోహం క్లోరిన్ తో రసాయనచర్య వలన బేరియం క్లోరైడ్ ఏర్పడును.
- Be + Cl2 → BeCl2
క్లోరిన్ సమక్షంలో బెరీలియం ఆక్సైడ్ను కార్బోథెర్మల్ రిడక్షన్ కావించడం వలన బేరియం క్లోరైడ్ ఏర్పడును.బెరీలియం లోహం హైడ్రోజన్ క్లోరైడ్ తో చర్య జరపడం వలన కూడా బేరియం క్లోరైడ్ ఏర్పడును.
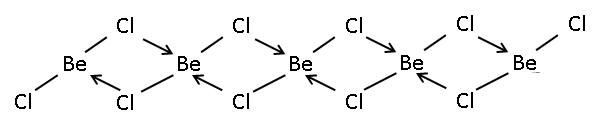
ఘన బేరియం క్లోరైడ్ అణువు చతుర్భుజాకార 1-ఏకమితి (1-dimensional)కలిగి, ఘన బేరియం క్లోరైడ్ పాలిమర్ సమూహం చతుర్కోణఅంచులను కలిగి ఉండును(పైన చిత్రంలో చూపిన విధంగా).
రసాయన చర్యలు
[మార్చు]తెమలేని పొడి గాలిలో బెరీలియం క్లోరైడ్ స్థిరమైనది. బెరీలియం క్లోరైడ్ ఒక లేవిస్ ఆమ్లం(Lewis acid).అందువలన సేంద్రియ రసాయనచర్యలలో బెరీలియం క్లోరైడ్ను ఉత్ప్రేరకం(catalyst )గా ఉపయోగిస్తారు. బెరీలియం క్లోరైడ్ జలవిశ్లేషణ వలన హైడ్రోజన్ క్లోరైడ్ ఏర్పడును:[4] BeCl2 + 2H2O → Be(OH)2 + 2HCl బెరీలియం క్లోరైడ్ టెట్రా హైడ్రేట్ (BeCl2•4H2O)ను ఏర్పరచును.ఈథర్ వంటి ఆక్సిజనరేటేడ్ ద్రావనులలో బెరీలియం క్లోరైడ్ కరుగుతుంది.
వినియోగం
[మార్చు]బెరీలియం లోహాన్ని విద్యుద్విశ్లేషణ విధానంద్వారా ఉత్పత్తి చెయ్యుటకై బెరీలియం క్లోరైడ్ ను ముడిసరుకుగా ఉపయోగిస్తారు. ఫ్రైడేల్-క్రాఫ్ట్స్ రసాయన చర్యలో బెరీలియం క్లోరైడ్ను ఉత్ప్రేరకంగా ఉపయోగిస్తారు.
ఇవికూడా చూడండి
[మార్చు]మూలాలు/ఆధారాలు
[మార్చు]- ↑ 1.0 1.1 "Beryllium Dichloride". pubchem.ncbi.nlm.nih.gov. Retrieved 2015-10-03.
- ↑ "SOME BERYLLIUM CHEMISTRY UNTYPICAL OF GROUP 2". chemguide.co.uk. Retrieved 2015-10-03.
- ↑ "Beryllium chloride". sigmaaldrich.com. Retrieved 2015-10-03.
- ↑ "BERYLLIUM CHLORIDE". cameochemicals.noaa.gov. Retrieved 2015-10-03.