లినొలిక్ ఆమ్లం

| |
| |
| పేర్లు | |
|---|---|
| IUPAC నామము
(9Z,12Z)-9,12-Octadecadienoic acid
| |
| ఇతర పేర్లు
C18:2 (Lipid numbers)
| |
| గుర్తింపు విషయాలు | |
| సి.ఎ.ఎస్. సంఖ్య | [60-33-3] |
| కెగ్ | C01595 |
| సి.హెచ్.ఇ.బి.ఐ | CHEBI:17351 |
| SMILES | CCCCC/C=C\C/C=C\CCCCCCCC(=O)O |
| |
| ధర్మములు | |
| C18H32O2 | |
| మోలార్ ద్రవ్యరాశి | 280.45 g·mol−1 |
| స్వరూపం | Colorless oil |
| సాంద్రత | 0.9 g/cm3[1] |
| ద్రవీభవన స్థానం | -50C [2] -12 0C [1] |
| బాష్పీభవన స్థానం | 2300C at 21 mbar[2] 2300C at 16 mmHg[1] |
| 0.139 mg/L[2] | |
| బాష్ప పీడనం | 16 Torr at 229 °C[ఆధారం చూపాలి] |
| ప్రమాదాలు | |
| జ్వలన స్థానం | {{{value}}} |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |
| Infobox references | |
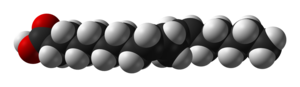
లినొలిక్ ఆమ్లం[3] అనునది నూనెలలో, కొవ్వులలో గ్లిసరైడు/గ్లిజరాయిడ్ (glyceride) రూపంలో లభించు ఒక అసంతృప్త కొవ్వు ఆమ్లం. కొవ్వు ఆమ్లాలను మోనోకార్బోక్సిల్ (Mono carboxyl) ఆమ్లమని అని కూడా ఆంటారు. ఎందు కనగా కొవ్వుఆమ్లం యొక్క ఉదజని-కర్బన శృంఖలం/గొలుసులో ఒక చివర మిథైల్ (CH3) [4] ఉండగా, రెండో చివర ఒక కార్బోక్సిల్ ( -C (=O) OH లేదా -COOH) [5] సమూహం మాత్రమే వుండటం వలన మోనో (మోనో అనగా ఒంటరి లేదా ఒకటి) కార్బోక్సిల్ ఆమ్లాలని అంటారు. లోనొలిక్ ఆమ్లం ఒక ఆవశ్యక కొవ్వు ఆమ్లం.
లినొలిక్ ఆమ్ల నిర్వచనము : కొవ్వు ఆమ్లం నిర్మాణంలో 18 కార్బనులను. కలిగి, సరళ హైడ్రోకార్బను శృంఖలయుతమై, శాఖారహితమై, రెండు ద్విబంధాలున్న కొవ్వుఆమ్లం.ఆమ్లం యొక్క హైడ్రోకార్బను శృంఖలం సరళ (straight) ముగా వుండి, శృంఖలంలోవున్న కార్బనుకు ఎటువంటి అదనపు హైడ్రోకార్బను శృంఖలం శాఖ (Branch) గా ఏర్పడి వుండదు. వ్యవహారిక పేరు లినొలిక్ ఆమ్లం కాగా శాస్త్రీయ పేరు సిస్, సిస్,9,12-ఆక్టాడెకాడైనోయిక్ ఆసిడ్ (cis, cis,9,12-Octadecadienoic acid).
లినొలిక్ ఆమ్ల నిర్మాణం[మార్చు]
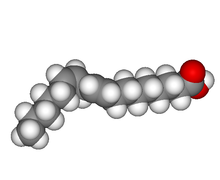
లినొలిక్ ఆమ్లం రెండు ద్విబంధాలను కలిగివున్న అసంతృప్త కొవ్వు ఆమ్లం. లినొలిక్ ఆమ్ల అణువు 18 కార్బనులను కలిగివున్నది. సాధారణ ఎంఫిరికల్ ఫార్ములా CnH2n-4O2.అనగా C18H32O2. లినొలిక్ ఆమ్లం కలిగి వున్న రెండు ద్విబంధాలను రెండు రకాలుగా వర్ణిస్తారు.
సిస్, సిస్-9,12 లినొలిక్ ఆమ్లం : దీనినే లినొలిక్ ఆమ్లం అంటారు. లినొలిక్ ఆమ్లం యొక్క హైడ్రోకార్బను శృంఖలంలో ఒక చివర మిథైల్ (CH3), రెండో చివర కార్బోక్సిల్ (COOH) గ్రూప్ వుండును. కార్బోక్సిల్ సమూహంలోని కార్బనును మొదటి కార్బనుగా మిథైల్ సమూహం వైపుకు శృంఖలంలోని కార్బనులను లెక్కించినచో 9వ కార్బను వద్ద మొదటి ద్విబంధం, 12 వకార్బను వద్ద రెండో ద్విబంధం ఏర్పడి వుండును. రెండు బంధాల వద్ద శృంఖలం మెలిక సిస్ అమరికలో సాధారణంగా వుండును. అలా రెండు బంధాలు సిస్ అమరికలో వున్న అది సాధారణ/అసలు లినొలిక్ ఆమ్లం. లినొలిక్ ఆమ్లం అనుపేరు సాధారణ పేరు. లినొలిక్ ఆమ్లం యొక్క శాస్త్రీయ పేరు cis, cis-9,12-Octadecadienoic acid అయ్యి ఉంది. లినొలిక్ ఆమ్లం యొక్క అణుభారం 280.4454.
ఒమేగా -6 కొవ్వు ఆమ్లం : కొవ్వు ఆమ్లం యొక్క హైడ్రోకార్బను శృంఖలం యొక్క మిథైల్ (CH3) సమూహంలోని కార్బనును మొదటి కార్బనుగా భావించి లెక్కించిన 6 వ కార్బను వద్ద ఆమ్లం యొక్క మొదటి ద్విబంధం ఏర్పడివుండటం వలన లినొలిక్ ఆమ్లాన్ని ఒమేగా -6 కొవ్వుఆమ్లమని కూడా పిలుస్తారు. లినొలిక్ ఆమ్లంలో మొదటి బంధం 6 వకార్బను వద్ద ఏర్పడగా, రెండో బంధం 9 వ కార్బను వద్ద ఏర్పడి వుండును (మిథైల్ సమూహం వైపునుండి లెక్కించినప్పుడూ). ఒమేగా-6 ఆమ్లంలో ద్విబంధం వద్ద అమరిక రెండు కూడా సిస్ (cis) అమరికలో వుండును. అయితే సాంకేతికంగా ఈ ఆమ్లాన్ని ఒమెగా-6-లినొలిక్ ఆమ్లమని పిలువవలెను. ఎందుకనగా ఏ కొవ్వు ఆమ్లం నైన మిథైల్ సమూహం నుంచి లెక్కించినప్పుడు 3వ కార్బను వద్ద ద్విబంధమున్న దాన్ని ఒమేగా-3 కొవ్వుఆమ్లమని, 6వ కార్బను వద్ద మొదటి ద్విబంధమున్న ఒమేగా-6 కొవ్వు ఆమ్లమని అంటారు.
సమాంగములు/ఐసొమరులు (isomers)[మార్చు]
ఒకేరకమమైన అణుసంకేతము/అణుసూత్రం (molecular formula) కలిగివుండి, బణువు (molecule) లోని అణువు (atom) ల అమరికలో వైవిధ్యం, భిన్నత్వం వున్నచో అట్టి సమ్మేళనాలను సమాంగములు లేదా ఐసొమరులు అంటారు. ఈ విధానాన్ని, లేదా రీతిని సమాంగతము (isomerism) అంటారు. లినొలిక్ ఆమ్లం యొక్క ఐసొమరులు ఉన్నాయి. లినొలిక్ ఆమ్లం యొక్క 28 సమాంగములు లేదా ఐసొమరులను గుర్తించారు[6].ఇవన్నియు లినొలిక్ ఆమ్లం యొక్క అనుబద్దిత సమాంగములు (conjugated isomers). లినొలిక్ ఆమ్లంలో ద్విబంధాలు 9,12 కార్బనుల వద్దవుండి, ద్విబంధ కార్బనుల వద్ద మెలిక ఒకటి సిస్, మరొకటి ట్రాన్సు అయిన దానిని లినొలిక్ ఆమ్లం యొక్క సమాంగం/ఐసోమరుగా భావించాలి.ఈ ఐసోమరు రెండు రకాలుగా ఏర్పడు అవకాశమున్నది.
- ట్రాన్సు, సిస్,9,12-అక్టాడిసెడైనోయిక్ ఆసిడ్ (trans, cis,9,12-octadecedienoic acid)
- సిస్, ట్రాన్సు,9,12-అక్టాడిసెడైనోయిక్ ఆసిడ్ (cis, trans,9,12-octadecedienoic acid)
- ట్రాన్సు, ట్రాన్సు,9,12-అక్టాడిసెడైనోయిక్ ఆసిడ్ (trans, trans,9,12-octadecedienoic acid)
పైన పేర్కొన్న సమాంగ నిర్మాణలున్న కొవ్వు ఆమ్లాలు, ఈ అమ్లాన్ని కలిగివున్న ట్రైగ్లిజరాయిడులను ఎక్కువ ఉష్ణోగ్రత వద్ద ఎక్కువ కాలం పదేపదే/పలుమార్లు వేడి చెయ్యడం వలనను, లేదా లినొలెనిక్ (Linolenic acid) ఆమ్లాన్ని పాక్షిక ఉదజనీకరణ చెయ్యునప్పుడు ఏర్పడును.
లినొలిక్ ఆమ్లం ఉనికి[మార్చు]
లినొలిక్ అనుపదం గ్రీకు పదమైన లినొన్ (linon) నుండి పుట్టినది. లినొన్ అనగా జనుము, ఒలిక్ . అనగా నూనెలకుకు సంబంధించిన లేదా వాటినుండి ఏర్పడినదని అర్థం.[7] లినొలిక్ ఆమ్లాన్ని 1923 లో ఆవశ్యక మైన పోషక పదార్థంగా గురించి, దానిని విటమిన్ 'ఎఫ్'గా వర్గీకరించారు. తిరిగి 1930 లో దీనిని నూనెలు, కొవ్వుఆమ్లాలలో చేర్చి ముఖ్యమైన మూడు ఆవశ్యక కొవ్వుఆమ్లాలలో ఒకటిగా గుర్తించారు. మిగిలిన రెండు లినొలెనిక్ (Linolenic acid) అమ్లం, అరచిడిక్ ఆమ్లం (Arachidic acid). లినొలెనిక్ కొవ్వుఆమ్లాన్ని ఒమేగా-3 కొవ్వుఆమ్లమని కూడా పిలుస్తారు.
లినొలిక్ ఆమ్లం భౌతిక గుణగణాలు[మార్చు]
లినొలిక్ ఆమ్లం సాధారణ ఉష్ణోగ్రత వద్ద ద్రవ రూపంలో వుండును. సాధారణంగా వర్ణరహితం (రంగు లేమి) గా లేదా నసు పసుపు రంగులో వుండును. జిడ్డుగా వుండును. దహించిన మండుతుంది. కళ్ళలో పడిన మండుతుంది. బలమైన ఆక్సీకరణ పదార్థములతో సులభంగా ఆక్సీకరణ చెందుతుంది. లినొలిక్ ఆమ్లం, సాధారణ వాతావరణం (760మి.మీ./పాదరస మట్ట పీడనం) లో 407-408 °C వద్ద బాష్పీభవనం చెందుతుంది. ద్రవీభవన ఉష్ణోగ్రత -12 °C. లినొలిక్ ఆమ్లం నీటిలో కరగదు. హైడ్రోకార్బను ద్రావణులలో కరుగుతుంది. ముఖ్యంగా హెక్సేను (hexane), క్లొరోఫారం (chloroform) ఇథైల్ ఈథరు (ethyl ether) లలో త్వరగా కరుగుతుంది. ఇథనాల్/ఎథనొల్ (ethanol) (ఇథైల్ ఆల్కహాల్) కరుగుతుంది, కాని ఉత్ప్రేరకం (catalyst) సమక్షంలో ఇథనాల్, మిథనాల్/మెథనోల్/మిథనల్ (methanol) లతో రసాయనిక చర్య జరుపుతుంది.
భౌతిక గుణగణల పట్టిక/జాబితా[8]
| గుణము | విలువల మితి |
| రూప స్థితి | ద్రవం |
| రంగు | రంగు లేదు, లేదా లేత పసుపు |
| విశిష్ట గురుత్వము | 0.902 కిలో/లీటరు |
| వక్రీభవన సూచిక | 1.4699 |
| భాష్ఫిభవన ఉష్ణోగ్రత | 407.85 °C |
| ద్రవీభవన ఉష్ణోగ్రత | (-5) °C |
| ఫ్లాష్ పాయింట్ | 110 °C |
రసాయన చర్యలు[మార్చు]
లినొలిక్ ఆమ్లం ఉదజనీకరణ, ఆక్సీకరణ, సపొనిఫికెసను, ఆల్కహాలిసిస్ వంటి రసాయనిక చర్యలలో చురుకుగా పాల్గొంటుంది. అంతేకాదు దేహా జీవక్రియ (Metabolism) లో ప్రముఖ పాత్ర వహిస్తుంది. జీవక్రియ సమయంలో అరచిడోనిక్ ఆమ్లం (Arachidonic acid=AA) ఏర్పడుటకు లినొలిక్ ఆమ్లం పూర్వగామి/అగ్రగామి (precursor) గా పనిచేస్తుంది. అక్కడి నుండి ప్రోస్టాగ్లాండిన్సు (prostaglandins) ఏర్పడుటకు తనవంతు పాత్ర పోషిస్తుంది.
ఉదజనీకరణం(hydrogenation)[9][మార్చు]
లినొలిక్ ఆమ్లాన్ని నికెల్ (nickel), లేదా పల్లాడియము (palladium) లోహాన్ని ఉత్ప్రేరకంగా ఉపయోగించి, అధిక వత్తిడి,, ఉష్ణోగ్రత వద్ద ఉదజని వాయువుతో చర్య నొందించినచో, ఉదజని లినొలిక్ ఆమ్లం యొక్క ద్విబందాలున్న కార్బను అణువులతో జతకట్టి/సంయోజనం చెంది, ద్విబంధాలను తొలగిస్తుంది. ఈ చర్యను ఉదజనీకరణం (hydrogenation) అంటారు. ఈ ఉదజనీకరణ రెండు రకాలుగా ఉంది. ఒకటి సంపూర్ణ ఉదజనికరణ అనగా Total hydrogenation లేదా complete hydrogenation. ఇక రెండవది పాక్షిక ఉదజనీకరణ (partial hydrogenation). దీన్ని అసంపూర్ణ ఉదజనీకరణ అనికూడా చెప్పవచ్చును.
సంపూర్ణ ఉదజనీకరణం: ఈ విధానంలో లినొలిక్ ఆమ్లాన్ని పూర్తిగా ఉదజనీకరణం చేయుదురు. లినొలిక్ ఆమ్లంలో వున్న రెండు ద్వింధాలలోని రెండు కార్బను అణువులతో లతో, నాలుగు ఉదజని అణువులు జతకూడటం వలన, కార్బనుల ద్విబంధం రద్దు అవ్వుతుంది. తత్ఫలితంగా లినిలిక్ ఆమ్లం సంతృప్త కొవ్వు ఆమ్లంగా పరివర్తన చెందుతుంది. లినొలిక్ ఆమ్లంలో 18 కార్బనులు వుండటం వలన, ఉదజణీకరణం తరువాత ఇది స్టియరిక్ ఆమ్లంగా మారుతుంది. ఈ విధంగా లినొలిక్ ఆమ్లాన్ని సంపూర్ణ ఉదజనీకరణ చర్యకు లోను కావించడం వలన స్టియరిక్ ఆమ్లం ఏర్పడుతుంది. స్టియరిక్ ఆమ్లం సాధారణ ఉష్ణోగ్రత వద్ద ఘన రూపంలో వుండును.
పాక్షిక లేదా అసంపూర్ణ ఉదజనీకరణం: పాక్షిక ఉదజనీకరణలో లినొలిక్ ఆమ్లంలోని రెండు ద్విబంధాలు ఏక బంధాలుగా మార్చబడవు. సంపూర్ణ ఉదజనీకరణం కంటే కన్న తక్కువ ప్రమాణంలో ఉదజని వాయువును లినొలిక్ ఆమ్లంతో రసాయనిక చర్య జరిపించడం వలన కొన్ని లినొలిక్ ఆమ్ల అణువులల్లో పాక్షికంగా మాత్రమే ఒక ద్విబంధం మాత్రమే తొలగింపబడుతుంది. కొన్నింటిల్లో రెండు ద్విబంధాలు తొలగింపబడగా, కొన్ని అణువులో రెండు ద్విబంధాలు అలాగే వుండిపోతాయి. అనగా పాక్షిక ఉదజనీకరణలో ఏర్పడిన ఉత్పతిలో మూడు రకాల సమ్మేళన పదార్థాలు వుంటాయి. ఒకటి రసాయన చర్యకు పూర్తిగా లోనయ్యి ఏర్పడిన స్టియరిక్ ఆమ్లం, రెండు చర్యకు లోనవ్వని లినొలిక్ ఆమ్లం,, ఒక ద్విబంధం మాత్రమే ఉదజనీకరణ చెందిన లినొలిక్ ఆమ్లం. లోనొలిక్ ఆమ్లంలో ఒకబంధం తొలగింపగా ఏర్పడిన ఆమ్లం ఒలిక్ ఆమ్లం కావొచ్చు లేదా దాని ఐసోమరు కూడా కావొచ్చును. ఒలిక్ ఆమ్లం బణువులో లోకూడా 18 కార్బనులు, ఒక ఏకద్విబంధం, 9 వ కార్బను వద్ద కలిగి, సిస్ అమరిక వుండును. ఇప్పడు పాక్షిక ఉదజనీకరణ వలన ఏక ద్విబంధంతో ఏర్పడిన కొవ్వుఆమ్లంలో కూడా 9 వ కార్బను వద్ద ద్విబంధం, సిస్ అమరిక వున్నచో అది ఒలిక్ ఆమ్లం. అలాకాకుండా 9 వ కార్బను వద్ద ద్విబంధమున్నప్పటికి సిస్ అమరికకు బదులుగా ట్రాన్సు అమరిక వున్నను, లేదా 9 వ కార్బను వద్ద ద్విబంధం తొలగింపబడి, 12 వకార్బను వద్దద్విబంధం కలిగి సిస్ లెదా ట్రాన్సు అమరిక వున్నచో అదికూడా లినిలిక్ ఆమ్లం యొక్క సమాంగత రూపనిర్మాణంగా భావించాలి.
పాక్షిక ఉదజనీకరణ వలన ఏర్పడు కొన్ని ఉత్పాదకాలు
- సిస్,9- అక్టాడిసెనొయిక్ ఆసిడ్: (cis,9-Octadecenoic acid) =ఒలిక్ ఆమ్లం
- ట్రాన్స్ - 9- అక్టాడిసెనొయిక్ ఆసిడ్: (Trans,9-Octadecenoic acid) =ఇలైడిక్ ఆమ్లం (Elaidic acid) ఒలిక్ ఆమ్లం యొక్క ఐసోమరు.
- సిస్,12-అక్టాడిసెనొయిక్ ఆసిడ్: (cis,12-Octadecenoic acid)
- ట్రాన్సు,12-అక్టాడిసెనొయిక్ ఆసిడ్: (Trans,12-Octadecenoic acid)
పైన పేర్కొన్న ఉత్పాదితాలు లేదా ఫలితాంశాలు యధేశ్చగా (randam) ఏర్పడినవేకాని ఇఛ్చాపూర్వకంగా (selective) గా ఏర్పడినవి కాదు.అందుచే ఒక పర్యాయం ఒక నిష్పత్తిలో ఏర్పడిన ఉత్పాదికములు మరో పర్యాయం కచ్చితంగా అదే నిష్పత్తిలో, అదే మాదిరిగా ఏర్పడే ఆవకాశం వుండవచ్చు లేదా నిష్పత్తి మారవచ్చును. పై విధంగా ఏర్పడిన పదార్థంలను అంశిక స్వేదనం (Fractional distillation) ద్వారా వేరుచెయ్యవచ్చును.
ఉదజనీకరణ ఊష్మాక్షేపక ప్రతిక్రియ (exothermic reaction). ఉదజణికరణ జరుగు సమయంలో చర్యాసమయంలో 105కిలో జౌల్/మోల్ ఉష్ణశక్తి వెలువడును.అందువలన చర్యాసమయంలో ఉష్ణోగ్ర్తత పెరుగుదలను గమనిస్తూ, నియంత్రణ కై తగుజాగ్రత్తలు తీసుకొనెదరు.
సాబునీకరణ (Saponification)[10][మార్చు]
ఆమ్లం, క్షారాలమధ్య చర్య వేగవంతంగా వుంటుంది.అందుచే కొవ్వుఆమ్లాలు క్షారాలతో (bases) అతిచురుకుగా రసాయనిక చర్యలో పాల్గొంటాయి. కొవ్వుఆమ్లాలు క్షారాలతో జరుపు రసాయనిక చర్య లేదా సంయోజనాన్నీసాబునీకరణ లేదా సపొనిఫికెసను అందురు.కారణం సోడియం,, పొటాషియం లతో ఏర్పడిన ఉత్పాదకాలను సబ్బు/సాబున్ గా ఉపయోగించుట వలన ఈ చర్యను సాబునీకరణ (సపొనిఫికెసను) అని పిలవటం సాధారణం.కొవ్వు ఆమ్లాలు బలహీన ఆమ్లాలు.సోడియం, పొటాషియం, లిథియం వంటివి బలమైన క్షారాలు. అందుచే ఈ రెండింటి సంయోగం వలన ఏర్పడు ఉత్ఫదికాలు క్షారగుణాలను అధికంగా కలిగి వుండును. అందువలన సబ్బులను కొవ్వుఆమ్లాల క్షారలవణాలని అనవచ్చును.
లినొలిక్ ఆమ్లం సోడియం/సోడియం హైడ్రాకైడ్ తో చర్య జరుపగా ఏర్పడిన ఏర్పడిన కొవ్వుఆమ్ల లవణాన్ని సోడియం లినొలియేట్ అనియు, పొటాషియం/పొటాషియం హైడ్రాకైడ్ చర్యతో ఏర్పడిన సాబునును/క్షారఅమ్ల లవణాన్నిపొటాషియం లినొలియేట్ అంటారు. లినొలిల్ ఆమ్లం క్షారాలతో పాటు వాటి యొక్క హైడ్రాక్సైడులతో, కార్బోనేటులతో, ఆక్సైడులతో కూడా చర్య జరుపును.
ఆల్కహాలిసిస్(Alcoholysis)[మార్చు]
సాధారణ ఉష్ణోగ్ర్త వద్ద లినొలిక్ ఆమ్లం ఆల్కహాలులలో కరుగుతుంది.ముఖ్యంగా మిథనాల్, ఇథనాల్, ప్రొపనాల్ వంటి ఆల్కహాలులలో.అల్కహాలుల ఉష్ణోగ్రతను పెంచిన లినిలిక్ ఆమ్లం త్వరితంగా కరుగుతుంది.ఒక్కడ లినొలిక్ ఆమ్లం ద్రావితం (solute,, ఆల్కహాలులు ద్రావణులు (solvents).ఒక సరియైన ఉత్ప్రేరకం సమక్షంలో (ఉదా:సల్ఫ్యూరిక్ ఆమ్లం, H2SO4) ఈ ద్రావిత, ద్రావణుల మధ్య రసాయనిక చర్యకు ప్రేరెపించిన ఆ చర్యను ఆల్కహాలిసిస్ అంటారు.చర్య ఫలితంగా ఈస్టరు/ఎస్టరులు ఏర్ఫడటం వలన ఎస్టరిఫికెసను (esterfication) అనికూడా అంటారు.ఈ విధంగా ఏర్పడిన ఉత్పాదకాలను కొవ్వుఆమ్లంయొక్క ఆల్కైల్ ఎస్టరులు అని అంటారు.
లినొలిక్ ఆమ్లాన్ని మిథనాల్ తో చర్య జరిపించిన మిథనాలిసిస్ (methanolysis) అనియు, ఏర్పడిన ఉత్పాదకాలను కొవ్వుఆమ్లాల మిథైల్ ఎస్టరులని అంటారు. ఇథైల్ ఆల్కహాల్ తో చర్య జరిపిన ఇథానాలిసిస్ (ethanolysis) అని, ఏర్పడిన ఉత్పాదకాలను కొవ్వుఆమ్లాల ఇథైల్ ఎస్టరులని అంటారు.
లినొలిక్ ఆమ్లాన్ని కలిగివున్న కొన్ని నూనెలు[మార్చు]
నూనె ఆమ్లశాతం నూనె ఆమ్లశాతం మిరపగింజల నూనె 73.0 కుసుమ నూనె 55.0-80.0 పొగాకుగింజల నూనె 64.0-67.0 సోయా నూనె 50.0-59.0 పుచ్చగింజల నూనె 63.0 ఖర్బుజగింజల నూనె 45.0-55.0 వెర్రిపుచ్చగింజల నూనె 50.0-52.0 టమాటోగింజల నూనె 50.0-54.0 ఒలిసలు నూనె 51.0-54.0 గోగుగింజల నూనె 46.0 తవుడు నూనె 39.0-40.0 నువ్వుల నూనె 35.0-50.0 రబ్బరుగింజల నూనె 36.0-37.0 బెండగింజల నూనె 34.0-39.0 జట్రొఫా నూనె 44.0 మోదుగ నూనె 19.0-22.0 బాదం నూనె 8.0-28 కుసుమ్ నూనె 21.0-25.0
జీవ క్రియ(metabolism)లో లినొలిక్ ఆమ్లం యొక్క పాత్ర[మార్చు]
లినొలిక్ ఆమ్లం జీవక్రియలో పాల్గొని జీవవ్యస్థకు, జీవ సంశ్లేషణ (biosynthesis) ద్వారాకు అవసరమైన ఎకోసనోయిడ్ (eicosanoid) లను Δ6డిస్యాచురేస్ (desaturase) ప్రమేయంతో ఏర్పరచును.ఈ Δ6డిస్యాచురేస్ అనునది ఒక ఎంజైము (Enzyme).ఇది జీవసంశ్లేషణ సమయంలో కొవ్వుఆమ్లంలోని కార్బను-కార్బనుమధ్య ఇథైల్ సమూహాన్ని సృష్టించడం ద్వారా కార్బనులమధ్య ద్విబంధాలను కల్గిస్తుంది.కార్బనుల మధ్య ఇథైల్ సముదాయం సహాయంతో, ద్విబంధాలను ఈ ఎంజైము పదేపదే ఏర్పరచగలదు.

Δ6డిస్యాచురేస్ ఎంజైం లినొలిక్ ఆమ్లంయొక్క హైడ్రోకార్బను గొలుసులోని కార్బనులమధ్య ఒక ద్విబంధాన్ని (12 వకార్బను) ఏర్పరచి, లినోలిక్ ఆమ్లాన్ని గామా-లినోలినిక్ ఆమ్లంగా మొదట మార్చుతుంది.తరువాత మరో ద్విబంధాన్ని ఏర్పరచడంద్వారా గామా-లినోలినిక్ ఆమ్లాన్ని20 కార్బనులు, మూడు ద్విబంధాలున్న డైహొమో గామా-లినోలినిక్ (dihomo gamma linolenic) ఆమ్లంగా మార్చుతుంది.ఈ డైహొమో ఆమ్లం 20 కార్బనులు, నాలుగు ద్బిబంధాలున్న అరాచిడోనిక్ ఆమ్లం (Arachidonic acid) గా మార్పుచెందుతుంది. అరాచిడోనిక్ ఆమ్లంనుండి జీవ సంశ్లేషణ వలన ఎకోసనోయిడులు ఉద్భవించును.ఎకోసనోయిడులు ఒక విధమైన పారక్రైన్ హర్మోనులు.
ఉపయోగాలు[మార్చు]
- జీవసంశ్లేషణ ద్వారా దేహవ్యవస్థలో ప్రోస్టగ్లాండినులను ఏర్పరచుతుంది,, కణపొరల (cell membrane) నిర్మాణంలో భాగం వహిస్తుంది.
- స్టియరిక్ ఆమ్లాన్ని తయారు చేయుదురు.
- జీవ ఇంధనం తయారు చేయవచ్చును.
- సబ్బులను, క్రీములను తయారు చేయుదురు.
ఇవికూడా చూడండి[మార్చు]
బహ్యా లింకులు[మార్చు]
మూలాలు[మార్చు]
- ↑ 1.0 1.1 1.2 The Merck Index, 11th Edition, 5382
- ↑ 2.0 2.1 2.2 2.3 మూస:GESTIS
- ↑ http://manatelugudoctor.blogspot.in/2013/10/aromatherapy-with-oils.html[permanent dead link]
- ↑ http://www.britannica.com/EBchecked/topic/378576/methyl-group
- ↑ "ఆర్కైవ్ నకలు". Archived from the original on 2014-07-10. Retrieved 2013-11-13.
- ↑ http://www.news-medical.net/health/What-is-conjugated-linoleic-acid.aspx
- ↑ "ఆర్కైవ్ నకలు". Archived from the original on 2013-03-28. Retrieved 2013-11-13.
- ↑ http://www.chemspider.com/Chemical-Structure.4444105.html
- ↑ "ఆర్కైవ్ నకలు". Archived from the original on 2013-11-18. Retrieved 2013-11-14.
- ↑ http://www.thefreedictionary.com/saponify
- All articles with dead external links
- మూలాలు చేర్చవలసిన పాఠ్యమున్న వ్యాసాలు
- మూలాలు చేర్చవలసిన పాఠ్యమున్న వ్యాసాలు from June 2011
- Chemical articles with unknown parameter in Chembox
- Articles containing unverified chemical infoboxes
- రసాయన శాస్త్రము మూసలు
- కొవ్వు ఆమ్లాలు
- అసంతృప్త కొవ్వు ఆమ్లాలు
- కర్బన సమ్మేళనాలు